Theo thông tin từ Bộ Y tế, từ 16 giờ ngày 19/12 đến 16 giờ ngày 20/12, Hệ thống Quốc gia quản lý ca bệnh COVID-19 ghi nhận 14.977 ca mắc mới, trong đó 11 ca nhập cảnh; 14.966 ca ghi nhận trong nước (giảm 1.127 ca so với ngày trước đó) tại 61 tỉnh, thành phố; có 9.000 ca trong cộng đồng.
Hà Nội tiếp tục là đia phương ghi nhận số ca mắc cao nhất nước với 1.612 ca, tiếp đó là Bến Tre (985 ca), Cà Mau (967 ca), Tây Ninh (947 ca)… Từ đầu dịch đến nay, Việt Nam có 1.555.455 ca mắc, 1.109.899 bệnh nhân đã được công bố khỏi bệnh; 29.791 ca tử vong.
Hiện, đang có 7.615 bệnh nhân nặng đang điều trị; trong đó, có 5.257 ca thở ô xy qua mặt nạ, 1.264 ca thở ô xy dòng cao HFNC, 166 ca thở máy không xâm lấn, 906 ca thở máy xâm lấn, 22 ca ECMO.
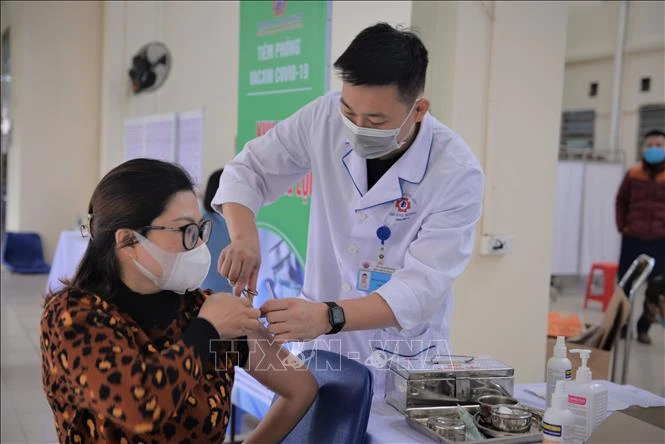
Tổng số vaccine đã được tiêm là 139.458.125 liều, trong đó tiêm mũi 1 là 75.889.748 liều, tiêm mũi 2 là 62.270.169 liều, tiêm mũi 3 (tiêm bổ sung/tiêm nhắc và mũi 3 của vaccine Abdala) là 1.298.208 liều.
Tăng cường kiểm tra, giám sát chất lượng thuốc điều trị COVID-19
Ngày 20/12, Cục Quản lý Dược, Bộ Y tế có văn bản khẩn gửi Sở Y tế các tỉnh, thành phố, Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh đề nghị tăng cường kiểm tra, giám sát chất lượng thuốc.
Cục Quản lý Dược cho biết, dịch COVID-19 đang diễn biến phức tạp, để ứng phó linh hoạt trong điều trị bệnh nhân COVID-19, Bộ Y tế đang tiếp tục xem xét, phê duyệt các thuốc và phác đồ điều trị nhằm đáp ứng kịp thời nhu cầu phòng, chống dịch.
Để đảm bảo an toàn cho người sử dụng, đồng thời đảm bảo việc cung ứng đủ thuốc chất lượng, an toàn, hiệu quả phục vụ cho hoạt động khám chữa bệnh, Cục Quản lý Dược đề nghị 63 Sở Y tế tiếp tục chỉ đạo các đơn vị trên địa bàn tăng cường kiểm tra, giám sát chất lượng thuốc trên thị trường trong giai đoạn dịch COVID-19.
Cục Quản lý Dược đề nghị Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh xây dựng kế hoạch, tăng cường việc lấy mẫu, kiểm tra chất lượng thuốc lưu hành trên thị trường, chú trọng việc lấy mẫu đối với các thuốc thuộc Danh mục thuốc kháng virus trong điều trị COVID-19 bao gồm các thuốc chứa hoạt chất Molnupiravir, Favipiravir, Remdesivir... sử dụng trong các chương trình nghiên cứu, thử thuốc trên lâm sàng trong điều trị COVID-19 theo các phác đồ của Bộ Y tế phê duyệt.
Riêng với thuốc Molnupiravir, Bộ Y tế cho biết từ giữa tháng 8 đến nay đã phân bổ 300.000 liều cho 46 địa phương để triển khai Chương trình sử dụng thuốc có kiểm soát thuốc này với F0 thể nhẹ tại cộng đồng. Nhiều địa phương như Hà Nội, Thành phố Hồ Chí Minh đưa Molnupiravir vào gói thuốc C, áp dụng với bệnh nhân COVID-19 điều trị tại nhà từ 18 tuổi trở lên.
Cập nhật, bổ sung kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 vaccine Nanocovax
Chiều 20/12, Bộ Y tế thông tin về cuộc họp xem xét báo cáo cập nhật, bổ sung kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 vaccine Nanocovax của Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia.
Bộ Y tế cho biết, ngày 16/12/2021, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia đã họp xem xét, đánh giá báo cáo cập nhật, bổ sung kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 ứng viên vaccine Nanocovax với kết quả nghiên cứu tính đến ngày 30/11/2021 (báo cáo nộp ngày 9/12/2021).
Trên cơ sở báo cáo, ý kiến của các thành viên, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia thống nhất kết luận: Vaccine Nanocovax đạt yêu cầu về tính an toàn tính dựa trên dữ liệu báo cáo bổ sung giữa kỳ phiên bản 8.0 ngày 30/11/2021.
Vaccine Nanocovax đạt yêu cầu về tính sinh miễn dịch theo Hướng dẫn chuyên môn về xem xét tính an toàn và hiệu quả bảo vệ phục vụ đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 của vaccine phòng COVID-19 sản xuất trong nước (ban hành kèm theo Quyết định 5259/QĐ-BYT ngày 11/11/2021 của Bộ trưởng Bộ Y tế) dựa trên dữ liệu báo cáo bổ sung giữa kỳ phiên bản 8.0 ngày 30/11/2021.
Về hiệu quả bảo vệ của vaccine, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia cho rằng, cần tiếp tục bổ sung dữ liệu các trường hợp mắc COVID-19 theo đề cương nghiên cứu đã được phê duyệt. Hội đồng cũng ghi nhận, đánh giá cao sự đóng góp của người tình nguyện tham gia nghiên cứu thử nghiệm lâm sàng vaccine COVID-19 nói chung, vaccine Nanocovax nói riêng. Đến nay, nghiên cứu thử nghiệm lâm sàng vaccine Nanocovax đã có đủ dữ liệu để đánh giá hiệu quả bảo vệ của vaccine nghiên cứu.
Tăng hạn dùng của vaccine Comirnaty
Bộ Y tế đã có Công văn số 10747/BYT-QLD gửi UBND các tỉnh, thành phố trực thuộc Trung ương về tăng hạn dùng của vaccine Comirnaty (Pfizer BioNTech COVID-19 Vaccine).
Trên cơ sở dữ liệu khoa học đánh giá độ ổn định của vaccine Comirnaty do Công ty trách nhiệm hữu hạn Pfizer (Việt Nam) cập nhật và sự phê duyệt của FDA, EMA và WHO, ngày 22/10/2021, Cục Quản lý Dược (Bộ Y tế) ban hành Công văn số 2926/QLD-KD về việc đồng ý tăng hạn dùng của vaccine Comirnaty ở điều kiện bảo quản từ -90oC đến -60oC.
Theo đó, hạn dùng của các lô vaccine có hạn dùng trên nhãn 6 tháng được cập nhật như sau: hạn sử dụng in trên bao bì là tháng 10/2021, tháng 11/2021, tháng 12/2021, tháng 1/2022, tháng 2/2022, tháng 3/2022 thì hạn dùng mới (tăng thêm 3 tháng) lần lượt là: tháng 1/2022, tháng 2/2022, tháng 3/2022, tháng 4/2022, tháng 5/2022, tháng 6/2022.
Việc tăng hạn dùng đối với vaccine Comirnaty (Pfizer BioNTech Covid-19 Vaccine) được áp dụng chung trên toàn cầu, không làm thay đổi chất lượng, an toàn, hiệu quả của vaccine, được sử dụng cho tất cả các đối tượng từ 12 tuổi trở lên.
Bộ Y tế đề nghị UBND các tỉnh, thành phố trực thuộc Trung ương chỉ đạo các đơn vị khẩn trương triển khai chiến dịch tiêm vaccine phòng COVID-19 năm 2021- 2022 theo đúng hướng dẫn của Bộ Y tế. Các lô vaccine Comirnaty (Pfizer BioNTech COVID-19 Vaccine) được tăng hạn nêu trên được sử dụng cho tất cả các đối tượng từ 12 tuổi trở lên.
Các địa phương cần đẩy mạnh truyền thông, tư vấn cho các đối tượng tiêm chủng, cha mẹ trẻ những thông tin đầy đủ về hạn dùng của vaccine nêu trên. Địa phương nào để vaccine hết hạn do không sử dụng mà phải tiêu hủy thì Giám đốc Sở Y tế phải hoàn toàn chịu trách nhiệm.
Triển khai ứng dụng y, dược cổ truyền trong phòng, chống dịch
Ngày 20/12, tại Hà Nội, Thứ trưởng Bộ Y tế Đỗ Xuân Tuyên đã chủ trì hội thảo Báo cáo, chia sẻ kinh nghiệm triển khai ứng dụng y, dược cổ truyền trong phòng, chống dịch COVID-19.
Thời gian qua, thuốc y học cổ truyền của Việt Nam đã tham gia vào điều trị và kết hợp với y học hiện đại để điều trị có kết quả cụ thể đối với nhiều trường hợp bệnh nhân mắc COVID-19.
Thông báo 226 về kết luận của Thủ tướng Chính phủ có nêu rõ yêu cầu kết hợp y học cổ truyền và y học hiện đại trong điều trị COVID-19. Bộ Y tế ban hành Quyết định 4539/QĐ-BYT ngày 25/9/2021 về hướng dẫn tạm thời sử dụng y dược cổ truyền trong phòng, điều trị COVID-19, đồng thời có công văn chỉ đạo Sở Y tế tại 63 tỉnh thành triển khai.
Trên tinh thần vừa làm vừa rút kinh nghiệm, qua mỗi đợt điều trị y học cổ truyền, các đơn vị cần làm tốt công tác báo cáo đánh giá những bài thuốc hay, phương thức điều trị hiệu quả và gửi đến Bộ Y tế. Cục Y, Dược cổ truyền phải chịu trách nhiệm thẩm định những ý kiến này, báo cáo với lãnh đạo Bộ Y tế.
Để có cở sở ứng dụng y, dược cổ truyền vào phòng, chống dịch COVID-19, Thứ trưởng Bộ Y tế đề nghị Cục Y, Dược cổ truyền phối hợp với Cục Khoa học công nghệ và các đơn vị liên quan xây dựng đề cương nghiên cứu, đưa ra các minh chứng, số liệu cụ thể, trình Bộ Y tế phê duyệt khẩn trong điều kiện "chống dịch như chống giặc".
Thứ trưởng Bộ Y tế nhấn mạnh đến việc áp dụng công nghệ thông tin trong việc theo dõi bệnh nhân đang điều trị ở nhà, đồng thời sử dụng truyền thông hiệu quả trong việc tuyên truyền về vận dụng y học cổ truyền trong điều trị COVID-19, tuyên truyền về những bài thuốc đã được tổng hợp có tác dụng phòng, chống COVID-19 để người dân hiểu và sẵn sàng áp dụng, sử dụng. Cục Y, Dược cổ truyền cần tổ chức tập huấn, cập nhật các bài thuốc hay cổ truyền để cán bộ y tế, người dân biết và sử dụng để phòng, chống COVID-19.
Các địa phương khẩn trương tiêm bổ sung và tiêm nhắc lại vaccine
Sở Y tế Hà Nội vừa ban hành Công văn số 22688/SYT-NVY về việc tiêm bổ sung và tiêm nhắc lại vaccine phòng COVID-19.
Theo đó, Sở Y tế yêu cầu Trung tâm Kiểm soát bệnh tật thành phố; Phòng y tế, Trung tâm y tế các quận/huyện/thị xã; các cơ sở khám, chữa bệnh trong và ngoài công lập đẩy nhanh hơn nữa tiến độ tiêm chủng vaccine phòng COVID-19 cho các đối tượng từ 12 tuổi trở lên, ưu tiên tiêm đủ liều cơ bản cho các đối tượng từ 50 tuổi trở lên, người có bệnh nền. Các đơn vị thực hiện rà soát đối tượng tiêm chủng, lập kế hoạch tiêm vaccine phòng COVID-19 theo đúng hướng dẫn của Bộ Y tế tại văn bản số 10722/BYT-DP ngày 17/12/2021.
Sở Y tế Đồng Tháp đề nghị các đơn vị phối hợp triển khai tiêm vaccine phòng COVID-19 liều bổ sung, liều nhắc lại giai đoạn 2021-2022. Theo đó, các sở, ban, ngành, đoàn thể, các tổ chức chính trị - xã hội tỉnh xây dựng kế hoạch, lập danh sách và cung cấp danh sách các đối tượng tiêm liều bổ sung, liều nhắc lại vaccine phòng COVID-19 theo quy định của Bộ Y tế về địa phương nơi đối tượng đang cư trú, lưu trú để cập nhật thông tin tổ chức tiêm cho các đối tượng; phối hợp tăng cường công tác truyền thông về lợi ích, tính an toàn của vaccine và những tác dụng không mong muốn có thể xảy ra sau khi tiêm để người dân hiểu rõ, hiểu đúng, tránh hoang mang và hưởng ứng chiến dịch tiêm chủng vaccine phòng COVID-19.
Theo kế hoạch tổ chức tiêm liều bổ sung, liều nhắc lại vaccine phòng COVID-19 trên địa bàn năm 2021 – 2022, UBND tỉnh Khánh Hòa đặt ra yêu cầu đẩy nhanh tiến độ bao phủ vaccine cho người dân, tăng cường miễn dịch phòng dịch COVID-19 cho những người đã được tiêm chủng đủ liều cơ bản.
PV