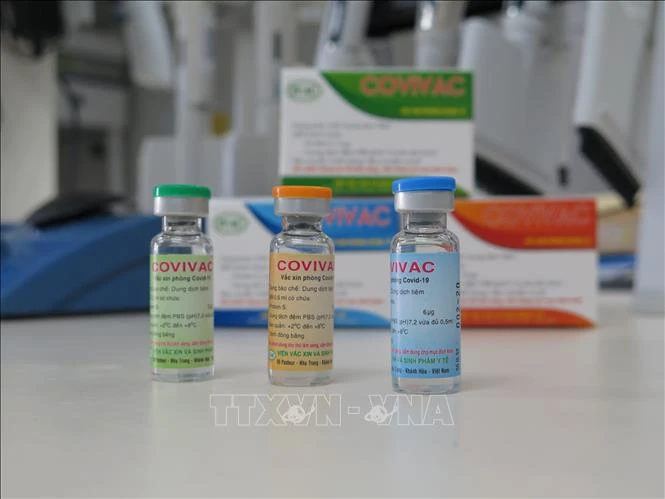
Phó Giáo sư, Tiến sĩ Vũ Đình Thiểm, Giám đốc Trung tâm Thử nghiệm lâm sàng, Viện Vệ sinh Dịch tễ Trung ương cho biết, ngày 15/9, nhóm nghiên cứu bắt đầu tiêm thử nghiệm mũi 2 giai đoạn 2 vaccine COVID-19 Covivac tại tỉnh Thái Bình. Dự kiến trong ngày 15/9 sẽ tiêm cho khoảng 80 người tình nguyện (riêng buổi sáng đã tiêm được trên 50 người).
Lộ trình tiêm mũi 2, giai đoạn 2 vaccine COVID-19 Covivac sẽ tiến hành từ nay đến ngày 20/9. Dự kiến sẽ tiêm cho 374 người tình nguyện (đây là những người đã tiêm mũi 1 đủ 28 ngày).
Giai đoạn 2 của thử nghiệm lâm sàng triển khai tại huyện Vũ Thư, Thái Bình với số lượng 375 tình nguyện viên, tiêm 2 nhóm liều 3mcg và 6 mcg và vaccine AstraZeneca (thay vì giả dược như lần 1).
Vaccine Covivac do Viện Vaccine và sinh phẩm y tế (IVAC) nghiên cứu, phát triển.
Theo Tiến sĩ Dương Hữu Thái, Viện trưởng Viện IVAC, đơn vị này đang chuẩn bị xây dựng đề cương thử nghiệm lâm sàng giai đoạn 3. Cuối tháng 9, nhóm nghiên cứu sẽ xin ý kiến chuyên gia góp ý đề cương này.
Sau khi có kết quả đánh giá tính an toàn và tính sinh miễn dịch ở giai đoạn 2 để xác định được liều tối ưu, dự kiến tháng 12/2021 sẽ bắt đầu triển khai thử nghiệm lâm sàng giai đoạn 3.
Theo dự kiến, giai đoạn 3 sẽ triển khai trên 4.000 đối tượng ở 3 tỉnh Khánh Hoà, Bắc Ninh và Thái Bình. Trong đó có nhóm đối chứng sử dụng một loại vaccine đã được cấp phép.
Phó Cục trưởng Cục Khoa học công nghệ và Đào tạo (Bộ Y tế) Nguyễn Ngô Quang cho biết, dự kiến, đến cuối năm 2021 sẽ có kết quả phục vụ đăng ký lưu hành vaccine phòng COVID-19 trong nước, ít nhất sẽ có 1 vaccine sản xuất trong nước được cấp phép lưu hành. Hiện Việt Nam đang có 3 ứng viên vaccine phòng COVID-19 đang triển khai nghiên cứu thử nghiệm lâm sàng.
Với vaccine Nano Covax - loại vaccine đầu tiên được cấp phép thử nghiệm lâm sàng ở Việt Nam, Phó Cục trưởng Cục Khoa học Công nghệ và Đào tạo cho biết, cuối giờ chiều 14/9, theo yêu cầu của Bộ Y tế, nhà sản xuất và nhóm nghiên cứu vaccine Nano Covax nộp hồ sơ hoàn thiện, bổ sung về thử nghiệm lâm sàng và đăng ký vaccine Nano Covax.
Với ARCT-154 chuyển giao công nghệ từ Mỹ, lãnh đạo Bộ Y tế đã cho phép triển khai cuốn chiếu giai đoạn 2 và giai đoạn 3 của vaccine này. Sau khi họp với nhóm nghiên cứu, việc triển khai thử nghiệm lâm sàng không chỉ thực hiện tại Hà Nội và Thành phố Hồ Chí Minh, mà sẽ được mở rộng địa bàn nghiên cứu ở khu vực phía Bắc gồm Bắc Ninh, Bắc Giang, Hải Dương, Hưng Yên; ở phía Nam gồm Đồng Nai, Tiền Giang, An Giang, Long An để đảm bảo tiến độ triển khai trước 20/12/2021 phải có đủ dữ liệu thử nghiệm lâm sàng giai đoạn 1, 2, 3.
Liên quan vaccine chuyển giao công nghệ, hiện Công ty Cổ phần Tiến bộ Quốc tế (AIC) và Công ty trách nhiệm hữu hạn một thành viên Vắcxin và Sinh phẩm số 1 (VABIOTECH) đã ký thỏa thuận bảo mật thông tin với Công ty Shionogi (Nhật Bản) để tiếp cận hồ sơ chuẩn bị triển khai thử nghiệm lâm sàng giai đoạn 3 tại Việt Nam và chuyển giao công nghệ sản xuất vaccine Recombinant SARS-CoV-2 Spike Protein (BaculovirusExpression Vector System).
Trước mắt Công ty Shionogi tập trung vào việc chuẩn bị cho thử nghiệm lâm sàng giai đoạn 3 vaccine này tại Việt Nam nên các công việc liên quan đến các bước tiếp theo trong việc chuyển giao công nghệ sản xuất vaccine này đang tiếp tục đàm phán.
Ngoài ra, Việt Nam đã có ký kết với vaccine HYPRA của Tây Ban Nha; dự kiến khởi động hợp tác nghiên cứu vào ngày 20/9. Vaccine này có công nghệ tương tự vaccine Nano Covax, hy vọng năm 2022 có kết quả tích cực.
Minh Huệ