Ngày 15/7, Bộ Y tế đã có quyết định số 3448/QĐĐ-BYT phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 đối với vaccine phòng COVID-19 Janssen.
Theo đó, căn cứ đề xuất của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đối với vaccine sinh phẩm tại cuộc họp ngày 4/7/2021 về dữ liệu chất lượng, an toàn và hiệu quả của vaccine do Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) cung cấp; đề nghị của Cục trưởng Cục Y tế dự phòng, Cục trưởng Cục Quản lý Dược, Cục trưởng Cục Khoa học Công nghệ và Đào tạo, Bộ Y tế phê duyệt có điều kiện vaccine cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 theo quy định tại Điều 67 Nghị định số 54/2017/NĐ-CP của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược.
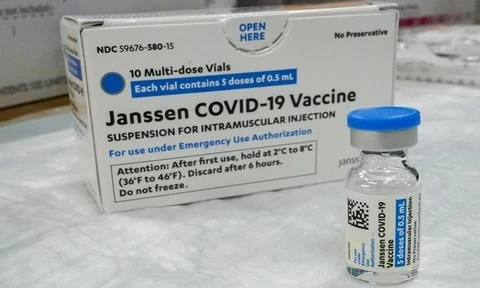
Tên vaccine là: COVID-19 Vaccine Janssen. Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều 0,5ml chứa Adenovirus chủng 26 được mã hóa glycoprotein cầu gai của SARS-CoV-2 (Ad26.COV2-S), lượng không nhỏ hơn 8,92 log10 đơn vị nhiễm khuẩn (Inf.U). Dạng bào chế: Hỗn dịch tiêm. Quy cách đóng gói: Hộp chứa 10 lọ; mỗi lọ đa liều 2,5ml chứa 5 liều.
Tên cơ sở sản xuất - Nước sản xuất: Janssen Pharmaceutica NV - Bỉ và Janssen Biologics B.V - Hà Lan.
Cơ sở đề nghị phê duyệt vaccine là Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam).
Quyết định của Bộ Y tế cũng nêu rõ, Cục Quản lý Dược có trách nhiệm cấp phép nhập khẩu vaccine COVID-19 Janssen theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu; thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vaccine nhập khẩu.
Cục Khoa học công nghệ và Đào tạo có trách nhiệm lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vaccine trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng. Cục hướng dẫn, chỉ đạo đơn vị có đủ điều kiện quy định tại Điểm a Khoản này tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của vaccine COVID-19 Janssen trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Cục Y tế Dự phòng thực hiện các trách nhiệm liên quan đến tiêm chủng vaccine COVID-19 Vaccine Janssen được quy định tại Quyết định số 1464/QĐ-BYT của Bộ trưởng Bộ Y tế về việc ban hành hướng dẫn tiếp nhận, bảo quản, phân phối và sử dụng vaccine phòng COVID-19 và Quyết định số 1467/QĐ-BYT của Bộ trưởng Bộ Y tế về việc phê duyệt kế hoạch tiêm vaccine phòng COVID-19 giai đoạn 2021 - 2022.
Viện Kiểm định Quốc gia vắc xin và sinh phẩm y tế có trách nhiệm tiến hành kiểm định và cấp Giấy chứng nhận xuất xưởng lô vaccine COVID-19 Janssen trước khi đưa ra sử dụng.
Như vậy, đến nay Bộ Y tế phê duyệt có điều kiện 6 loại vaccine cho nhu cầu cấp bách trong phòng, chống dịch COVID-19 gồm: vaccine Astra Zeneca; vaccine Sputnik; vaccine Pfizer; vaccine Vero Cell và vaccine Spikevax (Tên khác là: COVID-19 Vaccine Moderna) và Vaccine Janssen.
Cũng theo Bộ Y tế, vaccine COVID-19 Janssen được phê duyệt dựa trên dữ liệu an toàn, chất lượng và hiệu quả do Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) cung cấp cho Bộ Y tế Việt Nam tính đến ngày 03/7/2021 và cam kết của Công ty Trách nhiệm hữu hạnJohnson & Johnson (Việt Nam) về tính chính xác của các tài liệu đã cung cấp cho Bộ Y tế Việt Nam.
Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) có trách nhiệm phối hợp với cơ sở sản xuất vaccine phản hồi kịp thời các yêu cầu từ Bộ Y tế Việt Nam để bổ sung thêm dữ liệu hoặc các yêu cầu khác có liên quan đến vaccine COVID-19 Janssen và chủ động cung cấp, cập nhật các thông tin mới có liên quan đến vaccine COVID-19 Janssen cho Bộ Y tế Việt Nam trong suốt quá trình phát triển sản phẩm.
Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) chịu trách nhiệm phối hợp với cơ sở sản xuất vaccine đảm bảo các điều kiện sản xuất tại cơ sở sản xuất vaccine COVID-19 Janssen nhập khẩu vào Việt Nam và đảm bảo an toàn, hiệu quả và chất lượng của lô vaccine COVID-19 Janssen nhập khẩu vào Việt Nam.
Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) phối hợp với đơn vị phân phối, sử dụng vaccine COVID-19 Janssen triển khai hệ thống cảnh giác dược toàn diện đối với vaccine này tại Việt Nam theo quy định của pháp luật.
Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) phải phối hợp với Cục Khoa học công nghệ và Đào tạo và đơn vị có đủ điều kiện tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của Vaccine Janssen trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vắc xin, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Công ty Trách nhiệm hữu hạn Johnson & Johnson (Việt Nam) phải phối hợp với Bộ Y tế Việt Nam để triển khai quản trị rủi ro đối với vaccine COVID-19 Janssen trong suốt quá trình lưu hành tại Việt Nam. Việc sử dụng vaccine COVID-19 Janssen phải theo hướng dẫn của Bộ Y tế Việt Nam.
PV